
Brugada tipo I en paciente estable: Reporte de caso
Brugada type I in a stable patient: A case report
[Artículo en español / Article in Spanish]
Vol. 9 Núm. 4. Agosto 2025 - Octubre 2025.
e-ISSN: 2530-5468 - Open Access Journal
DOI: 10.5281/zenodo.17256751
Published under Creative Commons CC BY-NC-ND 4.0
Sanum. vol. 9, número 4 (2025) páginas 64 – 70
AUTORES:
Isabella Patiño Lemos MD, Universidad Libre Seccional Cali, Santiago de Cali, Colombia.
María Mercedes Menco Menco MD, Clínica Cali, Santiago de Cali, Colombia.
Juan Pablo Garaicoa Garzón MD, Especialista en medicina de urgencias, clínica nuestra señora de los remedios, Santiago de Cali, Colombia
Como citar este artículo:
Patiño-Lemos I, Menco-Menco MM, Garaicoa-Garzón JP.Brugada tipo I en paciente estable: reporte de caso. SANUM 2025, 9(4) pp 64 – 70 DOI: 10.5281/zenodo.17256751
© Los autores. Publicado por SANUM: Revista Científico-Sanitaria bajo una licencia Creative Commons Atribución-NoComercial-SinDerivadas 4.0 Internacional (CC BY-NC-ND 4.0). ![]()
How to cite this article:
Patiño-Lemos I, Menco-Menco MM, Garaicoa-Garzón JP. Brugada type i in a stable patient: a case report. SANUM 2025, 9(4) pp 64 – 70 DOI: 10.5281/zenodo.17256751
© The authors. Published by SANUM: Revista Científico-Sanitaria under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0). ![]()
Tipo de artículo: caso clínico.
Sección: Cardiología.
Fecha recepción: 25-08-2025
Fecha aceptación: 03-10-2025
Fecha publicación: 31-10-2025
RESUMEN
El síndrome de Brugada es una canalopatía hereditaria de alta relevancia clínica, asociada con arritmias ventriculares potencialmente letales y muerte súbita. Desde su primera descripción en 1992, esta condición ha evolucionado y se diagnostica mediante un patrón electrocardiográfico característico en las derivaciones precordiales derechas. El objetivo de este reporte de caso es describir el manejo integral de un paciente estable de 59 años con patrón de Brugada tipo I, enfatizando la importancia de una evaluación temprana y el uso de estrategias terapéuticas basadas en la evidencia. Se realizó una revisión de la literatura utilizando bases de datos como PubMed, centrándose en estudios recientes sobre la patogenia, estratificación del riesgo y tratamiento del síndrome. Los principales hallazgos incluyen la detección del patrón de Brugada tipo I en el EKG, la confirmación diagnóstica mediante un estudio electrofisiológico percutáneo que evidenció la inducibilidad de arritmias, y la implantación de un desfibrilador cardioversor implantable bicameral como medida preventiva definitiva. Se concluye que la detección oportuna y el manejo adecuado, con la colaboración estrecha entre urgenciólogos, cardiólogos y electrofisiólogos, son esenciales para reducir el riesgo de eventos arrítmicos mayores y mejorar la supervivencia de los pacientes afectados.
PALABRAS CLAVE:
Síndrome de Brugada;
Electrocardiograma;
Arritmia;
Desfibriladores Implantables;
Electrofisiología.
ABSTRACT:
Brugada syndrome is a hereditary channelopathy of high clinical significance, associated with potentially lethal ventricular arrhythmias and sudden cardiac death. Since its initial description in 1992, this condition has evolved and is now diagnosed based on a characteristic electrocardiographic pattern in the right precordial leads. The objective of this case report is to describe the comprehensive management of a stable 59-year-old patient presenting with a Brugada type I pattern, emphasizing the importance of early evaluation and the implementation of evidence-based therapeutic strategies. A literature review was conducted using databases such as PubMed, focusing on recent studies addressing the pathogenesis, risk stratification, and treatment of Brugada syndrome. The principal findings include the detection of the Brugada type I pattern on the electrocardiogram (ECG), diagnostic confirmation through a percutaneous electrophysiological study (EPS) that demonstrated arrhythmia inducibility, and the subsequent implantation of a dual-chamber implantable cardioverter-defibrillator (ICD) as a definitive preventive measure. In conclusion, timely detection and appropriate management—facilitated by close collaboration among emergency physicians, cardiologists, and electrophysiologists—are essential to reduce the risk of major arrhythmic events and improve patient survival.
KEYWORDS:
Brugada Syndrome;
Electrocardiography;
Arrhythmias, Cardiac;
Defibrillators, Implantable;
Electrophysiology.
INTRODUCCIÓN:
Desde su primera descripción en 1992, el síndrome de Brugada ha evolucionado notablemente, pasando de ser una mera curiosidad electrocardiográfica a convertirse en una entidad clínica compleja y de gran relevancia en la cardiología moderna. Inicialmente reconocido como una canalopatía hereditaria que predisponía a arritmias ventriculares y muerte súbita, este síndrome se diagnosticaba principalmente mediante la presencia de un patrón electrocardiográfico atípico, caracterizado por una elevación del segmento ST en las derivaciones precordiales derechas. Sin embargo, con el transcurso de los años, se ha evidenciado que la patogenia del síndrome de Brugada es multifactorial, integrando tanto alteraciones en la repolarización como en la despolarización, lo que a su vez ha permitido identificar diversos marcadores diagnósticos y pronósticos (1,2,3).
En primer lugar, cabe destacar la importancia de las mutaciones en el gen SCN5A, responsables de la codificación del canal de sodio cardíaco, aunque investigaciones posteriores han implicado además hasta 18 genes adicionales en la patogenia de la enfermedad. De igual manera, la heterogeneidad genética y fenotípica ha generado desafíos en la estratificación del riesgo, razón por la cual se han desarrollado diversas puntuaciones de riesgo que incorporan tanto hallazgos electrocardiográficos como clínicos. Asimismo, estudios recientes han puesto de relieve el papel del retraso en la conducción del tracto de salida del ventrículo derecho (TSVD) como predictor de eventos arrítmicos mayores. En este contexto, el signo aVR positivo y la onda S grande en la derivación I han emergido como marcadores prometedores, ya que reflejan de manera sencilla y no invasiva la presencia de alteraciones en la conducción que predisponen a arritmias graves (2,4,5).
Por otro lado, a pesar de los avances logrados, aún persisten interrogantes en cuanto a la interpretación de patrones electrocardiográficos transitorios o inducidos farmacológicamente, lo que evidencia la necesidad de seguir profundizando en la investigación clínica y electrofisiológica. Además, es fundamental integrar nuevos métodos diagnósticos, como el mapeo electroanatómico y la magnetocardiografía, que pueden complementar la información obtenida mediante el ECG tradicional (4,5,6).
En definitiva, el conocimiento acumulado durante más de tres décadas no solo ha permitido ampliar la comprensión del síndrome de Brugada, sino que también ha sentado las bases para mejorar la estratificación del riesgo y optimizar las estrategias terapéuticas, con el objetivo último de reducir la incidencia de eventos arrítmicos mayores y la mortalidad asociada a esta compleja enfermedad (5,7,8).
UN ENFOQUE INTEGRAL:
El síndrome de Brugada constituye una enfermedad hereditaria poco frecuente, pero de alta relevancia clínica, puesto que predispone a los pacientes a arritmias cardíacas potencialmente letales. En cuanto a la etiología, la primera asociación genética se identificó con una mutación de pérdida de función en el gen SCN5A, responsable del canal de sodio dependiente de voltaje; esta alteración se encuentra presente en aproximadamente el 15–30 % de los casos. Además, se han vinculado mutaciones en los canales de calcio y potasio, así como en proteínas asociadas y desmosómicas, lo que amplía el espectro genético de esta entidad. Es importante señalar que el síndrome de Brugada se hereda de forma autosómica dominante, aunque la expresividad variable y la penetrancia incompleta confieren un fenotipo altamente heterogéneo. Asimismo, diversos factores ambientales y farmacológicos, como la temperatura, ciertas medicaciones, las anomalías electrolíticas e incluso el consumo de cocaína, pueden modular la manifestación clínica de la enfermedad (1,2,3,4).
En términos epidemiológicos, la prevalencia del síndrome de Brugada se sitúa entre 3 y 5 por cada 10.000 personas, siendo esta afección entre 8 y 10 veces más común en hombres que en mujeres, con una edad promedio de presentación de 41 años. Por consiguiente, el síndrome representa aproximadamente el 4 % de todas las muertes súbitas cardíacas, lo cual subraya su importancia clínica a pesar de su baja incidencia en la población general. De igual forma, estos datos epidemiológicos resaltan la necesidad de una detección temprana y una evaluación rigurosa para prevenir eventos fatales (1,4,5,6).
Desde el punto de vista fisiopatológico, se han propuesto dos modelos principales para explicar los mecanismos subyacentes a esta condición. En primer lugar, el modelo del trastorno de la repolarización postula que la disminución de la corriente de sodio en el epicardio del ventrículo derecho genera una muesca más pronunciada en el potencial de acción, diferencia que se refleja en el electrocardiograma y predispone al paciente a arritmias graves. Por otro lado, el modelo del trastorno de la despolarización sugiere que un retraso en la activación, debido a una conducción lenta en el tracto de salida del ventrículo derecho, constituye el factor determinante que explica tanto los hallazgos electrocardiográficos característicos como la vulnerabilidad arrítmica (1,6,8).
El manejo del síndrome de Brugada requiere, por tanto, una evaluación exhaustiva que incluya la realización de un electrocardiograma de 12 derivaciones y, en casos dudosos, la aplicación de pruebas de provocación farmacológica. Además, el tratamiento de elección en pacientes de alto riesgo consiste en la implantación de un desfibrilador automático implantable (DAI); asimismo, alternativas terapéuticas, tales como el uso de quinidina y la ablación por radiofrecuencia, han demostrado eficacia en determinados contextos. En este sentido, la coordinación de un equipo interprofesional integrado por cardiólogos, electrofisiólogos y asesores genéticos, resulta fundamental para optimizar los resultados y brindar una atención integral a los pacientes y a sus familias (6,7,8).
PRESENTACIÓN DE CASO:
Paciente de 59 años de edad, sin antecedentes cardiológicos relevantes, que acude al centro de atención primaria por un cuadro de dolor torácico típico, descrito como opresivo, de inicio súbito y con irradiación a la región escapular derecha. A pesar de la intensidad del síntoma, el paciente se mostraba clínicamente estable, sin evidencia de disnea, palpitaciones, síncope o signos de insuficiencia cardiaca, lo que se corroboró en la exploración física, en la cual se apreciaron pulsos periféricos palpables y una presión arterial dentro de límites aceptables. Ver Figura No.1.
En la anamnesis se destaca la carencia de antecedentes personales o familiares de enfermedad cardiaca, lo que, sumado a la presentación aguda, motivó la evaluación inmediata. El electrocardiograma (EKG) inicial, realizado en atención primaria, evidenció un ritmo sinusal regular con una frecuencia cardiaca de 60 latidos por minuto (lpm), eje eléctrico normal y intervalos dentro de los rangos esperados (intervalo PR de 160 milisegundos [ms], duración del complejo QRS de 90 ms y corrección del intervalo QTc de 420 ms). De manera sobresaliente, en las derivaciones precordiales derechas (V₁ y V₂, extendiéndose ocasionalmente a V₃) se observó el patrón característico de Brugada tipo I: se apreciaba una elevación cóncava del segmento ST de al menos 2 mm, que descendía progresivamente y culminaba en una onda T invertida, sin evidenciar ondas Q patológicas. Además, se verificó un complejo QRS estrecho, sin indicios de bloqueo de rama ni alteraciones en la repolarización en las demás derivaciones, lo que constituye un signo negativo que descarta otras alteraciones isquémicas o conductivas.
Las determinaciones de enzimas cardíacas, troponinas resultaron negativas, descartándose un síndrome coronario agudo. Asimismo, el ecocardiograma transtorácico (ETT) evidenció una insuficiencia mitral mínima, con el resto de las válvulas normales; se observó una dilatación discreta de la aurícula izquierda, un ventrículo derecho sin dilatación y con contractilidad conservada, y un ventrículo izquierdo que presentaba leve hipertrofia concéntrica y disfunción diastólica tipo I, manteniendo la función sistólica preservada. La ausencia de alteraciones significativas en la función sistólica y la contractilidad global constituyen signos negativos que respaldan la sospecha de una patología predominantemente iónica, y no estructural.
Ante estos hallazgos y la sospecha de una canalopatía hereditaria, se remitió al paciente a un centro de mayor complejidad para la realización de un estudio electrofisiológico percutáneo (EEP), que incluyó el abordaje endovascular de las cavidades derecha e izquierda. Durante el EEP, se registró un ritmo sinusal a 60 lpm, con intervalos de conducción atrio-his (AH) de 82 ms y his-ventricular (HV) de 41 ms. La estimulación auricular, aplicada en ciclos de 600, 500 y 425 ms, permitió alcanzar el periodo refractario del nodo auriculoventricular (NAV) sin inducir arritmias ni evidenciar saltos o ecos; la estimulación incremental en la aurícula, hasta alcanzar 280 lpm, fue negativa para la inducción de arritmias, observándose un bloqueo de Wenckebach a 190 lpm.
No obstante, mediante el protocolo basal de inducción se desencadenó una taquicardia ventricular polimórfica, la cual requirió desfibrilación. El paciente toleró el procedimiento sin complicaciones, motivo por el cual se indicó el implante de un dispositivo de desfibrilador cardioversor implantable (DCI) bicameral, realizado de forma intra hospitalaria, como medida preventiva definitiva.
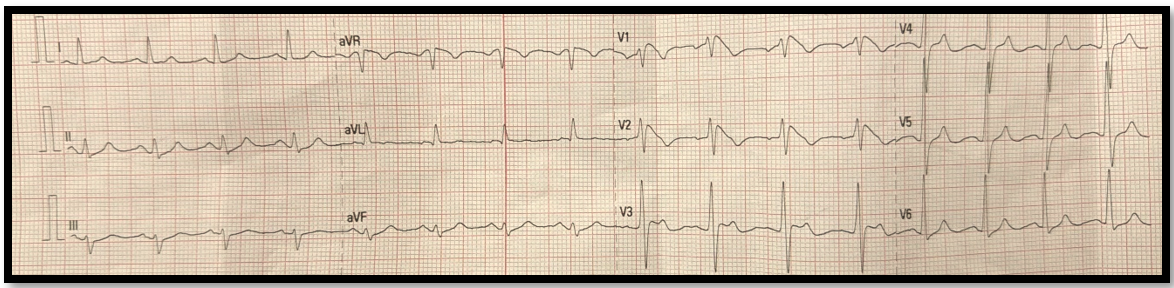
Figura No.1: Este EKG, al evidenciar de manera clara y uniforme el patrón de Brugada tipo I en las derivaciones precordiales derechas, resulta fundamental para el diagnóstico y manejo del síndrome. Dichos hallazgos, aun en un paciente clínicamente estable, son cruciales para orientar una evaluación más profunda y determinar estrategias terapéuticas específicas, tales como la consideración de pruebas de provocación o la implantación de un desfibrilador automático implantable en aquellos de alto riesgo. El EKG muestra ritmo sinusal a 100 lpm, PR 160 ms, QRS 90 ms, QTc 420 ms y eje normal. En V₁–V₃ se evidencia patrón de Brugada tipo I: elevación cóncava del ST ≥2 mm descendente a T invertida, sin ondas Q ni QRS ensanchado; las demás derivaciones son normales.(Fuente propia)
DISCUSIÓN:
El caso expone la relevancia clínica del síndrome de Brugada como entidad silenciosa con potencial arrítmico letal. El hallazgo electrocardiográfico de un patrón tipo I en derivaciones V₁–V₂ fue determinante para identificar riesgo de muerte súbita en un paciente sin antecedentes cardíacos aparentes. La inducibilidad de taquicardia ventricular polimórfica durante el estudio electrofisiológico (EEF) confirmó la indicación de un DCI bicameral, marcando una intervención preventiva de alto impacto. Este abordaje destaca el valor del EKG en la sospecha inicial y del EEF en la estratificación precisa del riesgo arrítmico.
Limitaciones de los estudios revisados: A pesar del respaldo en la literatura, las guías actuales presentan vacíos respecto a la interpretación de patrones intermitentes o atípicos de Brugada, así como sobre la utilidad universal del EEF en todos los pacientes con patrón tipo I espontáneo. Además, existe heterogeneidad en los criterios de riesgo según series clínicas, y muchas evidencias provienen de estudios retrospectivos o con muestras limitadas, dificultando la generalización de las estrategias terapéuticas.
Conexión entre los resultados y preguntas futuras: Este caso plantea interrogantes sobre el rol del mapeo electroanatómico y la genética molecular avanzada para refinar aún más la estratificación del riesgo. ¿Podrán estas herramientas diferenciar con mayor precisión qué pacientes con patrón tipo I aislado evolucionarán hacia eventos arrítmicos mayores? Asimismo, se requiere evaluar la indicación del EEF en pacientes con síntomas vagos o electrocardiogramas no concluyentes.
Implicaciones prácticas: Desde el punto de vista clínico, se refuerza la importancia de capacitar al personal de urgencias en la identificación de patrones Brugada, incluso en pacientes asintomáticos. Teóricamente, el caso reafirma el modelo de canalopatía con penetrancia incompleta, donde factores epigenéticos, ambientales o farmacológicos pueden desencadenar manifestaciones clínicas en sujetos genéticamente predispuestos. La integración multidisciplinaria, urgenciólogos, cardiólogos y electrofisiólogos— fue clave para lograr un desenlace favorable, y representa un estándar replicable en contextos de atención de riesgo arrítmico.
DISCUSSION
This case highlights the clinical relevance of Brugada syndrome as a silent entity with lethal arrhythmic potential. The electrocardiographic finding of a type I pattern in leads V₁–V₂ was decisive in identifying the risk of sudden cardiac death in a patient without an apparent cardiac history. The inducibility of polymorphic ventricular tachycardia during the electrophysiological study (EPS) confirmed the indication for a dual-chamber ICD, representing a preventive intervention of major impact. This approach underscores the value of the ECG in initial suspicion and the EPS in precise arrhythmic risk stratification.
Limitations of current evidence: Despite consistent support in the literature, current guidelines present gaps regarding the interpretation of intermittent or atypical Brugada patterns, as well as the universal applicability of EPS in all patients with spontaneous type I patterns. Furthermore, heterogeneity in risk criteria across clinical series and the predominance of retrospective or small-cohort studies limit the generalizability of therapeutic strategies.
Connection with future research: This case raises questions about the role of electroanatomical mapping and advanced molecular genetics in further refining risk stratification. Could these tools more precisely identify which patients with isolated type I patterns are likely to develop major arrhythmic events? Additionally, the indication of EPS in patients with vague symptoms or inconclusive electrocardiograms requires further evaluation.
Practical implications: From a clinical perspective, this case reinforces the importance of training emergency personnel to recognize Brugada patterns, even in asymptomatic patients. From a theoretical standpoint, it reaffirms the model of channelopathy with incomplete penetrance, in which epigenetic, environmental, or pharmacological factors may trigger clinical manifestations in genetically predisposed individuals. Multidisciplinary integration—including emergency physicians, cardiologists, and electrophysiologists—was essential to achieving a favorable outcome and represents a replicable standard in the management of arrhythmic risk.
CONCLUSIÓN:
El presente caso clínico resalta la importancia de reconocer el síndrome de Brugada tipo I aun en pacientes clínicamente estables, dado su potencial riesgo de arritmias ventriculares y muerte súbita.
El hallazgo electrocardiográfico característico en derivaciones precordiales derechas fue decisivo para orientar una evaluación más profunda y realizar un estudio electrofisiológico, que confirmó la susceptibilidad arrítmica. La implantación de un desfibrilador cardioversor bicameral constituyó la intervención preventiva definitiva, alineada con la evidencia actual.
Este caso subraya la necesidad de un abordaje integral y multidisciplinario, donde la colaboración entre urgenciólogos, cardiólogos y electrofisiólogos garantiza un diagnóstico oportuno y un tratamiento adecuado. Asimismo, enfatiza la relevancia de la educación médica para reconocer patrones electrocardiográficos sugestivos de Brugada en escenarios clínicos de primer contacto.
CONCLUSION
This clinical case underscores the importance of recognizing type I Brugada syndrome even in clinically stable patients, given its potential for life-threatening ventricular arrhythmias and sudden cardiac death.
The characteristic electrocardiographic pattern in right precordial leads was decisive in guiding further evaluation and prompted an electrophysiological study, which confirmed arrhythmic susceptibility. The implantation of a dual-chamber implantable cardioverter-defibrillator constituted the definitive preventive intervention, consistent with current evidence.
This case emphasizes the need for a comprehensive, multidisciplinary approach in which collaboration among emergency physicians, cardiologists, and electrophysiologists ensures timely diagnosis and appropriate treatment. It also highlights the relevance of medical education in recognizing electrocardiographic patterns suggestive of Brugada syndrome in frontline clinical settings.
DECLARACIÓN DE TRANSPARENCIA:
La autora principal (defensora del manuscrito) asegura que el manuscrito es un artículo honesto, adecuado y transparente; que ha sido enviado a la revista científica SANUM, que no ha excluido aspectos importantes del caso.
CONSENTIMIENTO INFORMADO
Se obtuvo el consentimiento informado por escrito de la paciente para acceso a historia clínica e información.
FINANCIACIÓN:
Los autores declaran que no recibieron apoyo financiero para la realización de la investigación ni para la publicación de este artículo.
CONFLICTOS DE INTERÉS:
Los autores manifiestan no tener relaciones comerciales o financieras que pudieran constituir un potencial conflicto de interés.
DECLARACIÓN SOBRE IA GENERATIVA:
Los autores afirman que no se utilizó inteligencia artificial generativa en la elaboración de este manuscrito.
CONTRIBUCIÓN DE LOS AUTORES:
IPL: Concepción del estudio, revisión bibliográfica, redacción inicial del manuscrito y aprobación final de la versión a publicar.
MMM: Recolección de datos clínicos, análisis crítico de la información, elaboración de la sección de discusión y aprobación final del manuscrito.
JPGG: Diseño metodológico, supervisión clínica del estudio, revisión crítica con aportes sustanciales al contenido científico y aprobación final de la versión a publicar.
BIBLIOGRAFÍA
- El Sayed M, Goyal A, Callahan AL. Brugada Syndrome. [Updated 2023 Aug 8]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK519568/
- Conte G, DE Asmundis C, Sieira J, Levinstein M, Chierchia GB, DI Giovanni G, Baltogiannis G, Ciconte G, Saitoh Y, Casado-Arroyo R, Pappaert G, Brugada P. Clinical characteristics, management, and prognosis of elderly patients with Brugada syndrome. J Cardiovasc Electrophysiol. 2014 May;25(5):514-519. doi: 10.1111/jce.12359. Epub 2014 Jan 21. PMID: 24400668.
- Eckardt, L., Veltmann, C. More than 30 years of Brugada syndrome: a critical appraisal of achievements and open issues. Herzschr Elektrophys 35, 9–18 (2024). https://doi.org/10.1007/s00399-023-00983-y
- Li KHC, Lee S, Yin C, Liu T, Ngarmukos T, Conte G, Yan GX, Sy RW, Letsas KP, Tse G. Brugada syndrome: A comprehensive review of pathophysiological mechanisms and risk stratification strategies. Int J Cardiol Heart Vasc. 2020 Jan 21;26:100468. doi: 10.1016/j.ijcha.2020.100468. Erratum in: Int J Cardiol Heart Vasc. 2020 Dec 19;32:100699. doi: 10.1016/j.ijcha.2020.100699. PMID: 31993492; PMCID: PMC6974766.
- Santoro, F., Di Biase, L., Curcio, A. et al. Psychological profile of patients with Brugada syndrome and the impact of its diagnosis and management. npj Cardiovasc Health 2, 3 (2025). https://doi.org/10.1038/s44325-024-00042-6
- Iqbal M, Putra ICS, Pranata R, Budiarso MN, Pramudyo M, Goenawan H, Akbar MR, Kartasasmita AS. Electrocardiographic Markers Indicating Right Ventricular Outflow Tract Conduction Delay as a Predictor of Major Arrhythmic Events in Patients With Brugada Syndrome: A Systematic Review and Meta-Analysis. Front Cardiovasc Med. 2022 Jun 17;9:931622. doi: 10.3389/fcvm.2022.931622. PMID: 35783830; PMCID: PMC9247269.
- Iqbal M, Putra ICS, Pranata R, Budiarso MN, Pramudyo M, Goenawan H, Akbar MR, Kartasasmita AS. Electrocardiographic Markers Indicating Right Ventricular Outflow Tract Conduction Delay as a Predictor of Major Arrhythmic Events in Patients With Brugada Syndrome: A Systematic Review and Meta-Analysis. Front Cardiovasc Med. 2022 Jun 17;9:931622. doi: 10.3389/fcvm.2022.931622. PMID: 35783830; PMCID: PMC9247269.
- Tse G, Liu T, Li KH, Laxton V, Chan YW, Keung W, Li RA, Yan BP. Electrophysiological Mechanisms of Brugada Syndrome: Insights from Pre-clinical and Clinical Studies. Front Physiol. 2016 Oct 18;7:467. doi: 10.3389/fphys.2016.00467. PMID: 27803673; PMCID: PMC5067537.

